Nebula Genomics DNA-Bericht für Epilepsie
Ist Epilepsie genetisch bedingt? Wir haben einen DNA-Bericht erstellt, der auf einer Studie basiert, die versucht hat, diese Frage zu beantworten. Unten sehen Sie einen SAMPLE DNA-Bericht. Kaufen Sie unseren, um Ihren personalisierten DNA-Bericht zu erhalten Sequenzierung des gesamten Genoms !

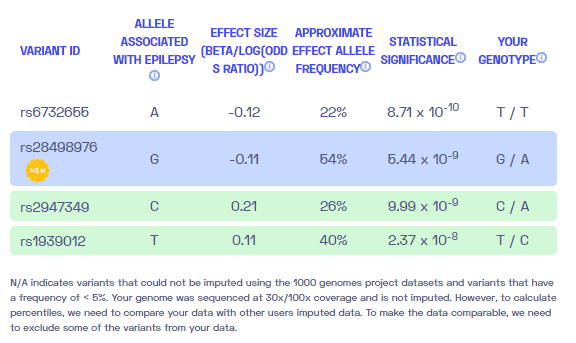
zusätzliche Information
Was ist Epilepsie? (Teil 1 von Ist Epilepsie genetisch bedingt?)
Epilepsie, manchmal als zerebrale Anfallsleiden oder zerebrale Krampfstörung bezeichnet, bezieht sich auf eine Hirnstörung mit mindestens einem spontan auftretenden epileptischen Anfall. Derzeit gibt es keine erkennbare Ursache (z. B. eine akute Entzündung des Gehirns, ein Schlaganfall oder eine Hirnverletzung / Kopfverletzung) oder einen Auslöser (z. B. Alkoholentzug bei bestehender Alkoholabhängigkeit oder massivem Schlafentzug).
Epilepsie ist eine chronische Erkrankung, die diagnostiziert werden kann, wenn nicht provozierte Anfälle mit einem erkennbar hohen Rezidivrisiko auftreten. Die Störung ist durch unvorhersehbare Anfälle gekennzeichnet und kann andere gesundheitliche Probleme verursachen. Es ist auch als Spektrum-Zustand mit einer Vielzahl von Anfallstypen und -kontrollen bekannt, die von Person zu Person variieren.
Biologisch gesehen ist ein epileptischer Anfall eine Folge plötzlicher, synchroner elektrischer Entladungen von Nervenzellen (Neuronengruppen) im Gehirn, die zu unwillkürlichen stereotypen Bewegungen oder psychischen Störungen führen. Die genaue Aktivität im Gehirn kann einzigartig sein. Der Ort des Ereignisses, wie es sich ausbreitet, wie stark das Gehirn betroffen ist und wie lange es dauert, hat tiefgreifende Auswirkungen.
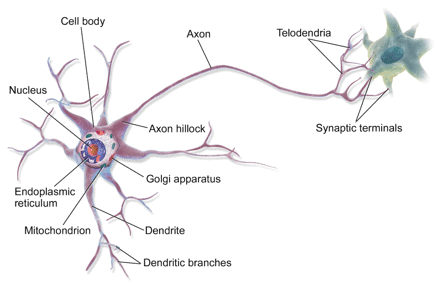
Für weitere Informationen die Epilepsie-Stiftung (copyright 2020) ist eine gemeinnützige Organisation, die Menschen mit Epilepsie helfen soll. Ihre Website ist voll von hilfreichen Informationen und Ressourcen.
Epidemiologie (Teil 2 von Ist Epilepsie genetisch bedingt?)
Laut der CDC Im Jahr 2015 hatten 1,2% der US-Bevölkerung (3,4 Millionen Menschen) aktive Epilepsie. Diese Zahl umfasst 3 Millionen Erwachsene und 470.000 Kinder mit Epilepsie.
Ein Erwachsener ab 18 Jahren leidet an aktiver Epilepsie, wenn er angibt, in der Vergangenheit eine vom Arzt diagnostizierte Epilepsie oder Anfallsleiden zu haben, und derzeit Medikamente zur Kontrolle einnimmt und / oder im vergangenen Jahr einen oder mehrere Anfälle hatte.
Ein Kind im Alter von 17 Jahren oder jünger leidet an aktiver Epilepsie, wenn seine Eltern oder Erziehungsberechtigten berichten, dass ein Arzt oder ein Gesundheitsdienstleister ihnen jemals mitgeteilt hat, dass sein Kind an Epilepsie oder Anfallsleiden leidet und wenn sein Kind derzeit an Epilepsie oder Anfallsleiden leidet.
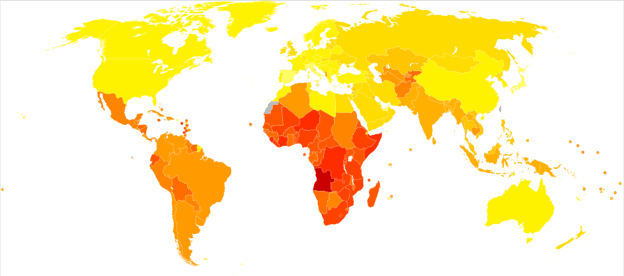
Epilepsie betrifft sowohl Männer als auch Frauen aller Rassen, ethnischen Hintergründe und Altersgruppen.
Symptome (Teil 3 von Ist Epilepsie genetisch bedingt?)
Wiederkehrende Anfälle sind ein Kennzeichen von Epilepsie. Die Anfallsymptome können zwischen den einzelnen Personen sehr unterschiedlich sein, obwohl die meisten Patienten mit Epilepsie dazu neigen, die gleichen Arten von Anfällen zu haben. Um als Epilepsie diagnostiziert zu werden, hat eine Person normalerweise mindestens zwei nicht provozierte Anfälle.
Mayo-Klinik stellt die häufigsten Symptome von Anfällen fest:
- Vorübergehende Verwirrung
- Ein starrender Zauber
- Unkontrollierbare Ruckbewegungen an Armen und Beinen
- Bewusstseinsverlust oder Bewusstseinsverlust
- Psychische Symptome wie Angst, Unruhe oder Deja Vu
Formen der Epilepsie können als eine von zwei Arten von Anfällen auftreten, fokale oder generalisierte.
Fokale Anfälle
Fokale Anfälle entstehen in einem Teil des Gehirns. Sie können ohne Bewusstseinsverlust auftreten, wenn der Patient veränderte Emotionen erfährt oder die Art und Weise verändert, wie Dinge aussehen, riechen, fühlen, schmecken oder klingen. Sie können auch ein unwillkürliches Zucken eines Körperteils wie eines Armes oder Beins und spontane sensorische Symptome wie Kribbeln, Schwindel und blinkende Lichter erfahren. Fokale Anfälle können auch bei Bewusstseinsstörungen auftreten, bei denen das Individuum entweder das Bewusstsein verliert oder sich seltsam gegenüber seiner Umgebung verhält, z. B. wenn es ausdruckslos starrt.
Generalisierte Anfälle
Generalisierte Anfälle betreffen das gesamte Gehirn. Sie sind in sechs Kategorien unterteilt:
- Abwesenheitsanfälle treten häufig bei Kindern auf und sind gekennzeichnet durch Starren in den Weltraum oder subtile Körperbewegungen wie Augenzwinkern oder Lippenklatschen.
- Tonische Anfälle führen zu einer Versteifung Ihrer Muskeln.
- Atonische Anfälle führen zu einem Verlust der Muskelkontrolle, was dazu führen kann, dass Sie plötzlich zusammenbrechen oder herunterfallen.
- Klonische Anfälle sind mit wiederholten oder rhythmischen, ruckartigen Muskelbewegungen verbunden. Diese Anfälle betreffen normalerweise Hals, Gesicht und Arme.
- Myoklonische Anfälle treten normalerweise als plötzliche kurze Rucke oder Zuckungen Ihrer Arme und Beine auf.
- Tonisch-klonische Anfälle sind die dramatischste Art von epileptischen Anfällen und können zu einem plötzlichen Bewusstseinsverlust, einer Versteifung und einem Zittern des Körpers und manchmal zu einem Verlust der Blasenkontrolle oder einem Zungenbiss führen.
Bei einigen Patienten ist das Risiko eines plötzlichen unerwarteten Todes bei Epilepsie (SUDEP) besorgniserregend. Der Tod tritt ohne andere zugrunde liegende Ursache ein und tritt normalerweise unmittelbar nach dem Auftreten eines Anfalls auf.
Ursachen der Epilepsie (Teil 4 von Ist Epilepsie genetisch bedingt?)
Obwohl das Wissen über die Entwicklung der Epilepsie in den letzten Jahrzehnten erheblich zugenommen hat, ist vieles noch unbekannt. Das Auftreten epileptischer Anfälle wird durch die Übererregbarkeit von Nervenzellen und die abnormale elektrische Aktivität größerer Nervenzellanordnungen im Gehirn verursacht. Es wird daher angenommen, dass ein Ungleichgewicht von Erregung und Hemmung in diesen neuronalen Netzen zu epileptischen Anfällen führt. Ungefähr 3 von 10 Menschen haben eine Veränderung in der Struktur ihres Gehirns, die die elektrischen Stürme von Anfällen verursacht.
Eine erhöhte Erregung oder verminderte Hemmung von Gehirnzellen kann sowohl durch Änderungen der Membraneigenschaften der Nervenstimulatorzellen als auch durch die Übertragung der Erregung von Nervenzelle zu Nervenzelle durch Neurotransmitter verursacht werden. Beispielsweise können Defekte in den Ionenkanälen für Natrium- und Calciumionen an der Erzeugung und Ausbreitung von Anfallsentladungen beteiligt sein.

Oft ist die Ursache von Anfällen mit dem Alter des Patienten verbunden. Die Epilepsiestiftung fasst zusammen, was bei Patienten unterschiedlichen Alters Anfälle auslöst:
Neugeborene können Anfälle aufgrund vorgeburtlicher Faktoren wie Fehlbildungen des Gehirns, Sauerstoffmangel während der Geburt, niedrigem Blutzuckerspiegel, Blutcalcium, Blutmagnesium oder anderen Elektrolytproblemen, angeborenen Stoffwechselstörungen, intrakraniellen Blutungen und mütterlichem Drogenkonsum haben. Säuglinge und Kinder sind am anfälligsten für Fieber, Hirntumor (selten) oder Infektionen (Narben im Gehirn).
Anfälle bei Kindern und jungen Erwachsenen werden am häufigsten durch angeborene Erkrankungen (Down-Syndrom; Angelman-Syndrom; Tuberkulose und Neurofibromatose), genetische Faktoren, fortschreitende Hirnkrankheiten (selten) oder Kopfverletzungen verursacht. Hirnschäden können in jedem Alter auftreten, sind jedoch bei jungen Erwachsenen am weitesten verbreitet und schwerwiegend. Bei Senioren ist Schlaganfall, Alzheimer oder Trauma höchstwahrscheinlich die Ursache.
Ist Epilepsie genetisch?
Einige Arten von Epilepsie treten in der Regel in Familien auf. Nicht alle Epilepsien aufgrund einer genetischen Ursache sind vererbte Epilepsie. Andere Typen können auf genetische Veränderungen zurückzuführen sein, die bei einem Individuum vererbt wurden oder zum ersten Mal auftraten. In solchen Fällen gab es möglicherweise keine Familiengeschichte mit Epilepsie.
Wenn eine Person ein enges Familienmitglied mit Epilepsie hat, besteht das Risiko, dass sie die Störung im Alter von 40 Jahren entwickelt weniger als 1 von 20 obwohl ein erhöhtes Epilepsierisiko besteht, wenn der Verwandte ersten Grades eher eine generalisierte Epilepsie als eine fokale Epilepsie hat.
Die ersten Gene im Zusammenhang mit Epilepsie wurden Ende der neunziger Jahre identifiziert. Fortschritte in der DNA-Sequenzierung haben jetzt Hunderte von Genen identifiziert, die bei Epilepsie eine Rolle spielen.
Einige davon Gene assoziiert mit Epilepsiestörung umfassen ALDH7A4, DEPDC5, EPM2A, GABARG2, GRIN2A, KCNQ2, LGI1, PCDH19, POLG, SCN1A und STXBP1.
Darüber hinaus kann Epilepsie auch bei Krankheiten auftreten, die auf einer Veränderung des Erbguts beruhen. In diesen Fällen ist der Anfall nur ein Symptom der Krankheit. Beispiele sind Tuberkulose oder Angelman-Syndrom.
Diagnose (Teil 5 von Ist Epilepsie genetisch bedingt?)
Zum Diagnose wird die Krankengeschichte von Menschen, die einen Anfall hatten, genommen. Ärzte versuchen zu verstehen, ob es sich bei dem Ereignis tatsächlich um einen echten Anfall handelte, ob es sich um einen Anfall handelte, ob es durch Epilepsie verursacht wurde und welche Art von Anfällen auftreten.
Die Patienten werden auch nach der Familienanamnese von Epilepsie, anderen Erkrankungen des Nervensystems und früheren Krankheiten, die symptomatische Epilepsie verursachen können, befragt. Dazu gehören Störungen und ein erhöhtes Risiko für Frauen mit Epilepsie während der Schwangerschaft, Probleme während der Geburt, die zu Sauerstoffmangel führen, Unfälle mit kraniozerebralen Traumata (Gehirnerkrankungen) oder entzündliche Erkrankungen des Zentralnervensystems.
Daran schließt sich eine körperliche Untersuchung, insbesondere des Nervensystems, an, bei der Kraft, Gefühl (Empfindlichkeit), Reflexe, Funktion des Hirnnervs, Gleichgewicht und Koordination untersucht werden.
Blutuntersuchungen werden auch verwendet, um mögliche Ursachen für symptomatische epileptische Anfälle (wie Hypoglykämie oder Mineralstoffmangel) zu identifizieren. Sie testen auch auf Anzeichen einer Nieren- oder Leberfunktionsstörung und andere häufige Probleme. Eine Lumbalpunktion (manchmal auch als Wirbelsäulenhahn bezeichnet) kann verwendet werden, um Infektionen wie Meningitis und Enzephalitis auszuschließen, und ein Toxikologie-Screening kann verwendet werden, um nach Toxinen zu suchen.
Typischerweise wird ein Elektroenzephalogramm durchgeführt. Die Bildgebung ist normalerweise Teil der Routinediagnose, während speziellere Verfahren speziellen Fragen vorbehalten sind.
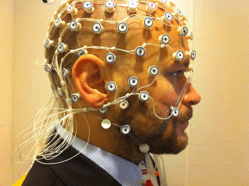
Elektroenzephalogramm (EEG)
Dies ist der häufigste Test für Epilepsie. Ein Computer zeichnet die elektrischen Muster des Gehirns des Patienten auf. Wenn Sie an Epilepsie leiden, kann das EEG abnormale Spitzen oder Wellen in den elektrischen Aktivitätsmustern des Gehirns aufweisen. Leider ist dieser Test nicht immer schlüssig, da viele Menschen mit Epilepsie zwischen den Anfällen normale EEGs haben.
Bildgebende Tests
Ein MRT- und ein CT-Scan sind bildgebende Tests, mit denen ein Arzt das Gehirn betrachten kann. Die Scans können Narbengewebe, Tumore oder strukturelle Probleme im Gehirn zeigen, die Anfälle oder Epilepsie verursachen können. Bildgebende Tests werden möglicherweise nicht nach einem ersten Anfall durchgeführt, sie werden jedoch in vielen Situationen empfohlen, z. B. nach einer Kopfverletzung.
Behandlung (Teil 6 von Ist Epilepsie genetisch bedingt?)
Die Behandlung besteht zunächst aus der Verabreichung von Medikamenten zur Unterdrückung von Anfällen (Antikonvulsiva). In therapieresistenten Fällen von Epilepsie werden auch andere Methoden wie die Epilepsieoperation angewendet. Epilepsie hat verschiedene Auswirkungen auf das tägliche Leben der betroffenen Person (z. B. Eignung für bestimmte Berufe oder Autofahren), die bei der Behandlung ebenfalls berücksichtigt werden müssen.
Medikamente
Die meisten Menschen können die Häufigkeit und Schwere von Anfällen mit anti-epliptischen Medikamenten reduzieren, und einige Menschen sehen einen vollständigen Stopp der Anfälle. Viele Menschen können die Medikation schließlich abbrechen, wenn keine Symptome vorliegen. Sie sollten immer Ihren Arzt konsultieren, bevor Sie Medikamente absetzen. Normalerweise werden Epilepsiemedikamente mit einer niedrigen Dosis begonnen und schrittweise erhöht.
Sie sollten Ihren Arzt unverzüglich benachrichtigen, wenn Sie neue oder verstärkte Depressionsgefühle, Selbstmordgedanken oder ungewöhnliche Veränderungen Ihrer Stimmung oder Ihres Verhaltens bemerken. Informieren Sie Ihren Arzt, wenn Sie an Migräne leiden, da diese möglicherweise eines der Antiepileptika verschreiben, das Ihre Migräne verhindern und Epilepsie behandeln kann.
Einige häufig Nebenwirkungen einschließen:
- Ermüden
- Schwindel
- Gewichtszunahme
- Verlust der Knochendichte
- Hautausschläge
- Verlust der Koordination
- Sprachprobleme
- Gedächtnis- und Denkprobleme
Schwerwiegendere, aber seltene Nebenwirkungen sind:
- Depression
- Selbstmordgedanken und Selbstmordverhalten
- Schwerer Ausschlag
- Entzündung bestimmter Organe, wie z. B. Ihrer Leber
In vielen Fällen sind diese Medikamente sehr wirksam und die Patienten werden anfallsfrei.
Chirurgie
Wenn Medikamente keine ausreichende Kontrolle über Anfälle bieten, kann eine Operation in Frage kommen. Bei dieser Operation entfernt ein Chirurg den Bereich des Gehirns, der Anfälle verursacht.
Sie können ein Kandidat für eine Operation sein, wenn die Anfälle in einem kleinen, genau definierten Bereich Ihres Gehirns auftreten und der zu operierende Bereich im Gehirn wichtige Funktionen wie Sprache, Sprache, Motorik, Sehvermögen oder Hören.
Oft können Patienten, die operiert werden, eine reduzierte Menge an Medikamenten einnehmen. In einigen wenigen Fällen kann eine Epilepsieoperation zu Komplikationen führen, z. B. zu einer dauerhaften Veränderung Ihrer kognitiven Fähigkeiten.
Alternative Therapien
Andere mögliche Therapien zur Behandlung von Anfällen wurden mit unterschiedlichem Erfolg eingesetzt. Diese Optionen umfassen:
- Vagusnervstimulation (ein Gerät ähnlich einem Schrittmacher)
- Ketogene Diät (Sie sollten einen Arzt konsultieren, wenn Sie oder Ihr Kind eine ketogene Diät in Betracht ziehen, da der Patient unterernährt werden kann, wenn er nicht richtig isst. Die Überwachung durch einen Ernährungsberater ist am besten.)
- Tiefenhirnstimulation (implantierte Elektroden im Gehirn)
Das United States National Institute of Neuorological Disorders and Stroke hat viele Ressourcen für Patienten sowie die Zentrum für Krankheitskontrolle und Prävention.
Wenn Ihnen dieser Artikel gefallen hat, sollten Sie unsere anderen Beiträge in der lesen Nebula Research Library !
