Nebula Genomics DNA Report for Epilepsy
A epilepsia é genética? Criamos um relatório de DNA com base em um estudo que tentou responder a essa pergunta. Abaixo você pode ver um relatório de amostra de DNA. Para obter seu relatório de DNA personalizado, adquira nosso Sequenciamento do genoma completo !

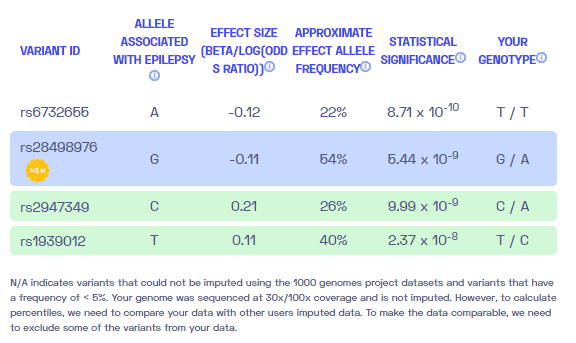
informação adicional
O que é epilepsia? (Parte 1 de A epilepsia é genética?)
A epilepsia, às vezes referida como distúrbio de convulsão cerebral ou distúrbio de espasmo cerebral, refere-se a um distúrbio cerebral com pelo menos uma crise epiléptica de ocorrência espontânea. Atualmente não existe uma causa identificável (como uma inflamação aguda do cérebro, um acidente vascular cerebral ou lesão cerebral / lesão na cabeça) ou gatilho (como a retirada do álcool no caso de dependência de álcool existente ou privação maciça de sono).
A epilepsia é um distúrbio crônico que pode ser diagnosticado quando ocorrem convulsões não provocadas com um risco reconhecidamente alto de recorrência. O distúrbio é caracterizado por convulsões imprevisíveis e pode causar outros problemas de saúde. É também conhecida como uma condição espectral com uma ampla variedade de tipos de crises e controle que varia de pessoa para pessoa.
Biologicamente, uma crise epiléptica é uma consequência de descargas elétricas síncronas e súbitas de células nervosas (grupos de neurônios) no cérebro, que levam a movimentos estereotipados involuntários ou distúrbios de saúde mental. A atividade exata no cérebro pode ser única. A localização do evento, como ele se espalha, quanto do cérebro é afetado e quanto tempo dura, todos têm efeitos profundos.
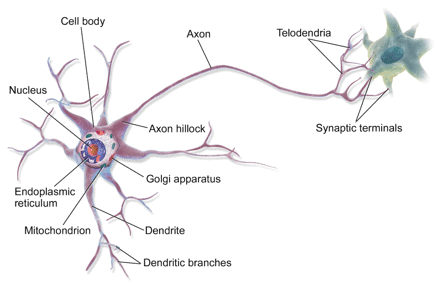
Para mais informações, o Epilepsy Foundation (copyright 2020) é uma organização sem fins lucrativos que visa ajudar pessoas com epilepsia. Seu site está cheio de informações e recursos úteis.
Epidemiologia (Parte 2 de A epilepsia é genética?)
De acordo com CDC , em 2015, 1,2% da população dos EUA (3,4 milhões de pessoas) tinha epilepsia ativa. Este número inclui 3 milhões de adultos e 470.000 crianças com epilepsia.
Um adulto com 18 anos ou mais tem epilepsia ativa se relatar que tem uma história de epilepsia ou distúrbio convulsivo diagnosticado pelo médico e está tomando medicamentos para controlá-lo e / ou teve um ou mais ataques no último ano.
Uma criança com 17 anos ou menos tem epilepsia ativa se seu pai ou responsável relatar que um médico ou profissional de saúde já disse que seu filho tinha epilepsia ou convulsão e se o filho atualmente tem epilepsia ou convulsão.
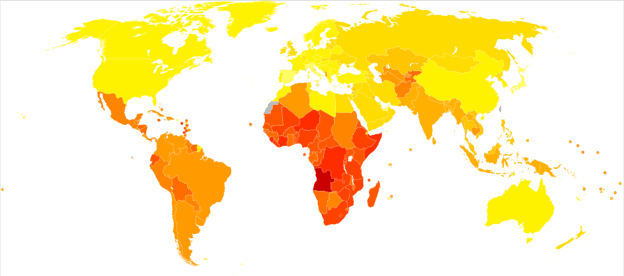
A epilepsia afeta homens e mulheres de todas as raças, origens étnicas e idades.
Sintomas (Parte 3 de A epilepsia é genética?)
Convulsões recorrentes são uma marca registrada da epilepsia. Os sintomas de convulsões podem variar muito entre os indivíduos, embora a maioria dos pacientes que vivem com epilepsia tendam a ter os mesmos tipos de convulsões. Normalmente, para ser diagnosticado como epilepsia, um indivíduo tem pelo menos duas crises não provocadas.
clínica Mayo observa os sintomas mais comuns de convulsões:
- Confusão temporária
- Um feitiço de olhar fixo
- Movimentos bruscos incontroláveis dos braços e pernas
- Perda de consciência ou percepção
- Sintomas psíquicos, como medo, ansiedade ou déjà vu
As formas de epilepsia podem aparecer como um de dois tipos de crises, focais ou generalizadas.
Ataques focais
As crises focais se originam em uma parte do cérebro. Eles podem ocorrer sem perda de consciência, onde o paciente experimenta emoções alteradas ou muda a aparência, o cheiro, a sensação, o sabor ou o som das coisas. Eles também podem sentir espasmos involuntários de uma parte do corpo, como um braço ou perna, e sintomas sensoriais espontâneos, como formigamento, tontura e luzes piscando. As crises focais também podem ocorrer com percepção prejudicada, em que o indivíduo perde a consciência ou se comporta de maneira estranha com o ambiente, como olhar fixamente para o vazio.
Convulsões generalizadas
As convulsões generalizadas afetam todo o cérebro. Eles são classificados em seis categorias:
- As crises de ausência costumam ocorrer em crianças e são caracterizadas por olhar para o vazio ou movimentos corporais sutis, como piscar os olhos ou estalar os lábios.
- As convulsões tônicas causam o enrijecimento dos músculos.
- As convulsões atônicas causam uma perda de controle muscular, o que pode fazer com que você desmaie ou caia repentinamente.
- As convulsões clônicas estão associadas a movimentos musculares espasmódicos repetidos ou rítmicos. Essas convulsões geralmente afetam o pescoço, o rosto e os braços.
- As convulsões mioclônicas geralmente aparecem como espasmos repentinos ou espasmos dos braços e pernas.
- As crises tônico-clônicas são o tipo mais dramático de crise epiléptica e podem causar uma perda abrupta de consciência, enrijecimento e tremor do corpo e, às vezes, perda do controle da bexiga ou morder a língua.
Para alguns pacientes, o risco de morte súbita inesperada em epilepsia (SUDEP) é uma preocupação. A morte ocorre sem qualquer outra causa subjacente e normalmente ocorre imediatamente após a ocorrência de uma convulsão.
Causas da epilepsia (Parte 4 de A epilepsia é genética?)
Embora o conhecimento sobre o desenvolvimento da epilepsia tenha aumentado significativamente nas últimas décadas, muito ainda é desconhecido. A ocorrência de ataques epilépticos é causada pela superexcitabilidade das células nervosas e pela atividade elétrica cerebral anormal de conjuntos maiores de células nervosas. Portanto, presume-se que um desequilíbrio de excitação e inibição nessas redes neurais leva a ataques epilépticos. Cerca de 3 em cada 10 pessoas têm uma alteração na estrutura de seus cérebros que causa as tempestades elétricas das convulsões.
O aumento da excitação ou diminuição da inibição das células cerebrais podem ser causadas por alterações nas propriedades da membrana das células estimuladoras dos nervos e na transmissão da excitação de uma célula nervosa para outra por neurotransmissores. Por exemplo, defeitos nos canais de íons para íons de sódio e cálcio podem participar da geração e propagação de descargas convulsivas.

Freqüentemente, a causa das convulsões está associada à idade do paciente. The Epilepsy Foundation resume o que desencadeia convulsões em pacientes de várias idades:
Os recém-nascidos podem ter convulsões devido a fatores pré-natais, como malformações cerebrais, falta de oxigênio durante o nascimento, níveis baixos de açúcar no sangue, cálcio no sangue, magnésio no sangue ou outros problemas eletrolíticos, erros inatos do metabolismo, hemorragia intracraniana e uso de drogas pela mãe. Bebês e crianças são mais suscetíveis a febre, tumor cerebral (raramente) ou infecções (cicatrizes no cérebro).
As convulsões em crianças e adultos jovens são mais comumente causadas por doenças congênitas (síndrome de Down; síndrome de Angelman; esclerose tuberosa e neurofibromatose), fatores genéticos, doença cerebral progressiva (rara) ou traumatismo craniano. Os danos cerebrais podem ocorrer em qualquer idade, mas são mais prevalentes e graves em adultos jovens. Em idosos, acidente vascular cerebral, doença de Alzheimer ou trauma são as causas mais prováveis.
Epilepsia é genética?
Alguns tipos de epilepsia tendem a ocorrer em famílias. Nem todas as epilepsias devido a uma causa genética são epilepsia hereditária. Outros tipos podem ser devidos a alterações genéticas que foram herdadas ou ocorreram pela primeira vez em um indivíduo. Nesses casos, pode não haver história familiar de epilepsia.
Se uma pessoa tem um familiar próximo com epilepsia, o risco de desenvolver o transtorno aos 40 anos é menos de 1 em 20 embora haja um risco aumentado de epilepsia se o parente de primeiro grau tiver epilepsia generalizada em vez de epilepsia focal.
Os primeiros poucos genes relacionados à epilepsia foram identificados no final da década de 1990. Avanços no sequenciamento de DNA já identificaram centenas de genes que desempenham um papel na epilepsia.
Alguns desses genes associados ao distúrbio de epilepsia incluem ALDH7A4, DEPDC5, EPM2A, GABARG2, GRIN2A, KCNQ2, LGI1, PCDH19, POLG, SCN1A e STXBP1.
Além disso, a epilepsia também pode ocorrer em doenças baseadas em uma mudança na composição genética. Nesses casos, a convulsão é apenas um sintoma da doença. Os exemplos são a esclerose tuberosa ou a síndrome de Angelman.
Diagnóstico (Parte 5 de A epilepsia é genética?)
Pra diagnóstico , é feito o histórico médico de pessoas que tiveram uma convulsão. Os médicos tentam entender se o evento foi de fato uma convulsão real, se foi uma convulsão, se foi causada por epilepsia e o tipo de convulsão que está ocorrendo.
Os pacientes também são questionados sobre a história familiar de epilepsia, outras doenças do sistema nervoso e doenças anteriores que podem causar epilepsia sintomática. Estes incluem distúrbios e risco aumentado para mulheres com epilepsia durante a gravidez, problemas durante o parto que levam à deficiência de oxigênio, acidentes com traumatismo craniocerebral (doenças cerebrais) ou doenças inflamatórias do sistema nervoso central.
Isso é seguido por um exame físico, especialmente do sistema nervoso, com exame de força, sensação (sensibilidade), reflexos, função dos nervos cranianos, equilíbrio e coordenação.
Os exames de sangue também são usados para identificar as possíveis causas das crises epilépticas sintomáticas (como hipoglicemia ou deficiência mineral). Eles também testam sinais de disfunção renal ou hepática e outros problemas comuns. Uma punção lombar (às vezes chamada de punção lombar) pode ser usada para descartar infecções, como meningite e encefalite, e um exame toxicológico pode ser usado para procurar toxinas.
Normalmente, um eletroencefalograma é realizado. A imagem geralmente faz parte do diagnóstico de rotina, enquanto procedimentos mais especializados são reservados para questões especiais.
Eletroencefalograma (EEG)
Este é o teste mais comum para epilepsia. Um computador registra os padrões elétricos do cérebro do paciente. Se você tem epilepsia, o EEG pode mostrar picos ou ondas anormais nos padrões de atividade elétrica do cérebro. Infelizmente, esse teste nem sempre é conclusivo porque muitas pessoas com epilepsia têm EEGs normais entre as crises.
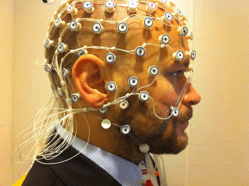
Testes de imagem
Uma ressonância magnética e uma tomografia computadorizada são exames de imagem que permitem ao médico visualizar o cérebro. As varreduras podem mostrar tecido cicatricial, tumores ou problemas estruturais no cérebro que podem causar convulsões ou epilepsia. Os testes de imagem podem não ser feitos após a primeira convulsão, mas são recomendados em muitas situações, como após um ferimento na cabeça.
Tratamento (Parte 6 de A epilepsia é genética?)
O tratamento consiste inicialmente na administração de medicamentos supressores de convulsões (anticonvulsivantes). Em casos de epilepsia resistentes à terapia, outros métodos, como a cirurgia de epilepsia, também são usados. A epilepsia tem uma variedade de efeitos na vida diária da pessoa afetada (como aptidão para certas profissões ou dirigir um carro), que também devem ser levados em consideração no tratamento.
Remédios
A maioria das pessoas pode reduzir a frequência e a gravidade das convulsões com medicamentos anti-eplípticos e algumas pessoas veem uma parada completa das convulsões. Muitas pessoas podem descontinuar a medicação na ausência de sintomas. Você deve sempre consultar seu médico antes de interromper qualquer medicamento. Normalmente, os medicamentos para epilepsia são iniciados com uma dose baixa e aumentados gradualmente.
Deve notificar o seu médico imediatamente se notar um novo ou um aumento da sensação de depressão, pensamentos suicidas ou alterações anormais no seu humor ou comportamento. Informe o seu médico se você tiver enxaquecas, pois eles podem prescrever um dos medicamentos antiepilépticos que podem prevenir suas enxaquecas e tratar a epilepsia.
Algo comum efeitos colaterais incluir:
- Fadiga
- Tontura
- Ganho de peso
- Perda de densidade óssea
- Erupções cutâneas
- Perda de coordenação
- Problemas de fala
- Problemas de memória e pensamento
Os efeitos colaterais mais graves, mas raros, incluem:
- Depressão
- Pensamentos e comportamentos suicidas
- Erupção cutânea severa
- Inflamação de certos órgãos, como o fígado
Em muitos casos, esses medicamentos são muito eficazes e os pacientes ficam livres das convulsões.
Cirurgia
Quando os medicamentos não conseguem controlar adequadamente as convulsões, a cirurgia pode ser uma opção. Nesta cirurgia, um cirurgião remove a área do cérebro que está causando as convulsões.
Você pode ser um candidato à cirurgia se as crises se originam em uma área pequena e bem definida do seu cérebro e a área do cérebro a ser operada não interfere nas funções vitais, como fala, linguagem, função motora, visão ou audição.
Freqüentemente, os pacientes submetidos à cirurgia podem tomar uma quantidade reduzida de medicamentos. Em um pequeno número de casos, a cirurgia para epilepsia pode causar complicações, como alterar permanentemente suas habilidades cognitivas.
Terapias alternativas
Outras terapias potenciais para tratar convulsões têm sido usadas com vários graus de sucesso. Essas opções incluem:
- Estimulação do nervo vago (um dispositivo semelhante a um marca-passo)
- Dieta cetogênica (você deve consultar um médico se você ou seu filho estiver considerando uma dieta cetogênica, pois o paciente pode ficar desnutrido se não comer adequadamente. A supervisão de um nutricionista é melhor)
- Estimulação cerebral profunda (eletrodos implantados no cérebro)
O Instituto Nacional de Transtornos Neurológicos e AVC dos Estados Unidos tem muitos Recursos para os pacientes, bem como o Centro de Controle e Prevenção de Doenças.
Se você gostou deste artigo, você deve verificar nossos outros posts no Nebula Research Library !
