Что такое эпигенетика?
Эпигенетика — это изучение факторов, определяющих активность ген в человеке геном . Он включает изменения в функции генов, которые не основаны на изменениях в ДНК последовательности, но передавались дочерним клеткам.
В основе эпигенетики лежат химические изменения хроматина. Это может повлиять на белки, которые связываются с ДНК, или на саму ДНК. Эти изменения могут влиять на активность участков или целых хромосом. Это также называется эпигенетическим изменением или эпигенетическим импринтингом.
Поскольку последовательность ДНК не изменяется, эпигенетические модификации не могут быть обнаружены в последовательности ДНК. Типы эпигенетических процессов включают инактивацию Х-хромосом, импринтинг гена или сохранение транскрипционной памяти клеток.
Под редакцией Кристины Сордс, доктора философии.
Основы эпигенетики
После оплодотворения яйцеклетка делится. До стадии 8 клеток все дочерние клетки равны. Их называют тотипотентными, потому что каждый из них сам по себе способен производить полноценный организм.
После этого этапа появляются клетки с другой внутренней программой. Эти клетки имеют ограниченный потенциал развития, поскольку они становятся все более и более специализированными.
Когда тело полностью сформировано, большинство клеток тела твердо запрограммированы на выполнение своих функций на основе эпигенетических механизмов. Функция была зафиксирована из-за биохимических модификаций оснований в ДНК или гистонов, упаковывающих ДНК, или того и другого. Последовательность генетического материала остается неизменной, за исключением нескольких случайных мутаций.
Такие эпигенетические модификации приводят к тому, что определенные участки генома «заглушаются», то есть не могут быть легко транскрибированы в РНК для синтеза белка. Эти модификации выглядят в соматических клетках совершенно иначе, чем в стволовых или половых клетках. Наиболее важными модификациями являются метилирование цитозиновых оснований и метилирование и ацетилирование боковых цепей гистонов.
Помимо метилирования, теломеры имеют важное эпигенетическое влияние. Теломеры защищают концы хромосом от деградации во время деление клеток . Фермент теломераза обеспечивает сохранность хромосом. Психический стресс может снизить активность этого фермента, что в конечном итоге привело к ускоренному укорачиванию теломер в процессе старения.
C сравнение к генетике
Термин эпигенетика можно понять, если рассмотреть процесс наследования:
- Перед делением клетки генетический материал удваивается. Затем половина дублированного генома переносится в одну из двух дочерних клеток. Половина материнского генетического материала доставляется яйцеклеткой, а отцовская половина — сперматозоидом.
- Молекулярная генетика описывает генетический материал как двойную спираль двух цепей дезоксирибонуклеиновой кислоты. Нити содержат фосфат-дезоксирибозный сахарный полимер в качестве основы. Генетическая информация поступает из последовательности четырех оснований, которые присоединены к остову сахара дезоксирибозы. Это аденин (A), цитозин (C), гуанин (G) и тимин (T).
- Основания одной нити почти всегда сочетаются с совпадающим основанием второй нити. Аденин соединяется с тимином, а цитозин — с гуанином.
- Генетическая информация закрепляется в порядке строительных блоков A, C, G, T (базовая последовательность).
Некоторые явления наследственности нельзя объяснить с помощью только что описанной модели ДНК:
- Во время дифференцировки клеток в процессе деления клеток образуются дочерние клетки с другой функцией. После дифференцировки клеток разные типы клеток все еще сохраняют сходные последовательности ДНК. Определение функциональной идентичности клетки — тема эпигенетики.
- Есть черты, которые «унаследованы» только от отца или матери и не связаны с ДНК. Нарушения этого состояния приводят к серьезным заболеваниям.
- Когда дифференцированные клетки снова трансформируются в стволовые, эпигенетические паттерны должны быть удалены. Клетка может снова приобрести и унаследовать все или многие функции, когда эпигенетические фиксации удалены.
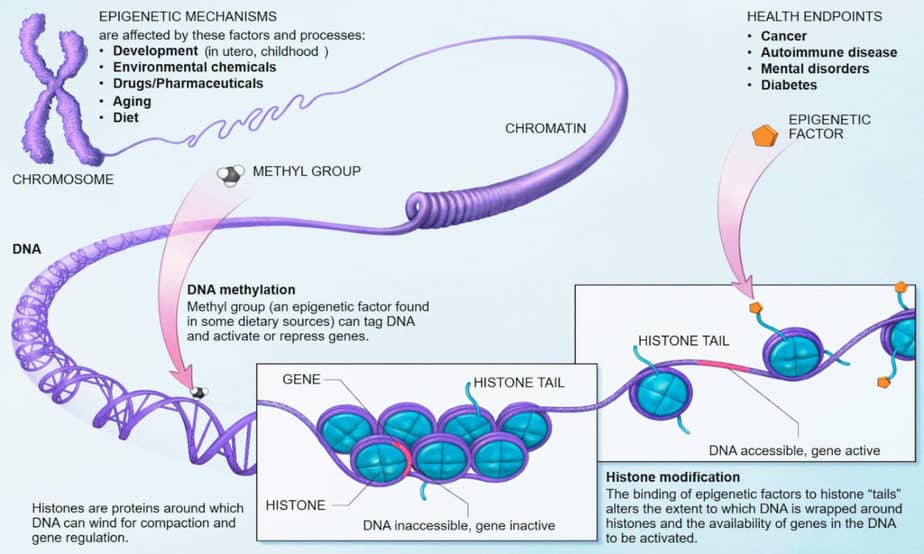
Гистоны и их роль в эпигенетической фиксации
ДНК не присутствует в ядре клетки голой, но связана с гистонами. Восемь различных гистоновых белков образуют ядро нуклеосомы, на котором намотаны 146 пар оснований цепи ДНК. Концы гистоновых цепей выступают из нуклеосомы и являются мишенью для ферментов, модифицирующих гистоны.
Модификации гистонов представляют собой в основном метилирование и ацетилирование лизина, гистидина или аргинина, а также фосфорилирование серинов. Также играет роль, занята ли боковая цепь лизина одной, двумя или тремя метильными группами. Своеобразный «гистоновый код» может быть связан с активностью генов, связанных гистонами.

Влияние метилирования и ацетилирования на конформацию хроматина
Изменения в боковых цепях гистонов изменяют объем генного сегмента. Есть меньшие объемы сегментов генов в закрытой конформации, наряду с конденсацией хромосом и инактивацией генов. Большие объемы генных сегментов можно наблюдать в открытой конформации наряду с генной активностью. Переход между двумя состояниями обусловлен присоединением и отщеплением метильных групп к основаниям цитозина.
В общем, присоединение ацетильных групп к гистонам приводит к раскрытию конформации нуклеосомы. Это открытие делает ген доступным для транскрипции с помощью РНК-полимеразы. Присоединение метильных групп к боковым цепям лизина приводит к присоединению метилсвязывающего белка MeCB, который подавляет экспрессию гена. Эти белки-репрессоры закрывают конформацию гистонов, предотвращая транскрипцию.
Эпигенетические изменения на жизненном пути
Эпигенетика не ограничивается случаями наследственности. Все больше внимания уделяется связи между происходящими изменениями в жизненном пути и развитием заболеваний. Например, однояйцевые близнецы демонстрируют высокую степень эпигенетического сходства в возрасте трех, но не 50 лет. У одного близнеца степень метилирования была в 2,5 раза выше.
Таким образом, несмотря на свою генетическую идентичность, старшие близнецы эпигенетически тем разнообразнее, чем более различается их жизненный путь. Причиной этого является не только окружающая среда, с которой они сталкиваются, но и неточность передачи паттернов метильных групп во время каждого деления клетки. Таким образом, в течение жизни постепенные изменения накапливаются все больше и больше.
Изменение рациона рабочих пчел вызывает в высшей степени эпигенетическое перепрограммирование генома личинок. Было идентифицировано более 500 генов, на которые влияют изменения метилирования, вызванные окружающей средой.
Активация или неактивация генов — не единственное последствие изменения диеты. Есть также альтернативный сплайсинг и продукты измененных генов.
Эпигенетические изменения как объяснение болезней
Объяснение факторов стресса является основным направлением эпигенетических исследований. Для этой цели использовались люди с ранним травматическим жизненным опытом, вызванным отсутствием ухода за беременными. Стресс запускает гормональный каскад, который начинается в гипоталамусе, части промежуточного мозга.
Было показано, что ген глюкокортикоида обнаруживает совершенно разные метилирования у соответствующих индивидуумов. Соответственно, ген подавляется при наличии стресса в анамнезе. Продукт гена в коре надпочечников, конечной станции гормональной цепи, впоследствии будет другим. В результате материнского поведения в головном мозге повышается или понижается регуляция более 900 генов.
Результаты были подтверждены и на людях. Ген рецептора в гиппокампе человека во многом идентичен гену других млекопитающих. Следовательно, эпигенетические изменения аналогичны таковым у крыс.
В исследовании с участием кандидатов-самоубийц пострадавшие разделились на две группы: с опытом жестокого обращения в детстве и без. Только у кандидатов с историей злоупотреблений ген рецептора был заблокирован метилированием.
Травма, полученная матерью во время беременности, может иметь для будущего ребенка долговременные последствия, которые будут длиться десятилетия. Существует значительный рост риска шизофрении и сердечных заболеваний у детей от матерей, пострадавших от голода. У этих детей также наблюдались изменения в характере метилирования гена Igf2.
У мышей регулярное потребление коки меняет эпигенетический паттерн нескольких сотен генов в центре вознаграждения мозга. Это увеличивает чувствительность к действию лекарств и увеличивает риск привыкания.
Масштабы эпигенетических изменений в течение жизни во много раз превышают масштабы генетических мутаций. Он может дать новые ответы на различные заболевания, такие как шизофрения, болезнь Альцгеймера, рак, диабет у взрослых, нервные расстройства и многие другие.
Наследование эпигенетических отпечатков
Открытия эпигенетических изменений, особенно в популярной науке, постоянно проводят параллели с ламаркизмом. Ламаркизм, или передача приобретенных характеров, рассматривается как противоречащий классической генетике.
Однако существует очень мало доказательств того, что приобретенные и приобретенные способности могут передаваться через половые клетки. Передача приобретенных способностей следующему поколению еще не является доказательством генетического проявления. Кроме того, термин «поколение» часто неверно истолковывают как начало индивидуального цикла.
Наследование эпигенетических отпечатков было предложено в 2003 году Рэнди Джиртлом и Робертом Уотерлендом с использованием экспериментов на мышах. Самкам мышей агути перед спариванием и во время беременности вводили определенный состав питательных веществ. Было обнаружено, что большая часть потомства не проявляла типичного фенотипа.
В исследовании на людях различные факторы, предоставившие информацию о доступности пищи и смертности в маленьком шведском городке Оверкаликс . Было обнаружено, что у большинства людей, чьи бабушки и дедушки резко изменили рацион питания, с возрастом развивались сердечно-сосудистые заболевания.
Однако болезнь развивалась по определенной схеме, которая предполагает эпигенетические изменения в половых хромосомах. Например, в семьях, где дедушка ел хорошо или слишком много, пострадали только внуки мужского пола.
Согласно гипотезе Уильяма Р. Райса и его коллег, эпигенетика может быть причиной человеческого гомосексуализма . Сексуальное предпочтение матери будет передано сыну, а предпочтение отца — дочери.
Это могло бы произойти, если бы эпигенетические маркеры генов, ответственных за сексуальную ориентацию, сохранялись в половых клетках. Если не удалить эпигенетические метки в яйцеклетке, эмбрион может иметь сексуальную ориентацию матери. Согласно этой гипотезе, гомосексуализм у человека врожденный.
Гипотеза объясняет, почему случаи гомосексуализма у людей остаются статистически стабильными с течением времени. Однако нет никаких эмпирических доказательств связи между гомосексуализмом и эпигенетикой.
